衰弱和抑郁症状可通过多模式干预(如力量训练和营养改善)进而降低心血管疾病发病风险

随着老龄化速度的增加,中老年人的健康状况成为越来越重要的关注点,伴随年龄增长而来的是不可避免的身体衰弱和社会活动减少,这些改变可能会引起心理上的压力和不适,从而对身体健康产生负面的叠加效应。不久前一篇发表在《自然·通讯》杂志上的高分文献便报道了这一现状,研究显示,衰弱和抑郁症状已成为老年人心血管疾病发病风险的重要影响因素,而积极的联合干预(身体活动+饮食干预+心理支持)可以显著减轻这种影响。

一 五大全球纵向队列数据库的联合研究
研究者选择全球具有代表性的五个权威数据库,通过数据筛选和清洗,选取50岁及以上且数据完整的参与者共76894人。结合多种Cox比例风险模型、中介分析、交叉滞后面板网络分析等方法,发现衰弱状态对心血管疾病的发生发展具有深远影响,且抑郁情绪的持续会扩大这一负面影响。

该研究发表于2025年6月,题为《Frailty and depressive symptoms in relation to cardiovascular disease risk in middle-aged and older adults》。在研究过程中,作者团队排除了慢性合并症、相关药物、失访、死亡、混杂偏倚等因素对研究潜在的干扰,以科学的手段证明了针对衰弱和抑郁症状的综合干预措施对预防老年人群心血管疾病的必要性。
二 功能医学如何看待“衰老—抑郁—疾病”之间的关系
不同于急性发炎(红肿热痛,旨在清除病原体),炎性衰老是一种低度、慢性、无菌性、系统性的炎症状态。随着年龄增长,这种背景噪音般的炎症水平逐渐升高。它的源头在哪里?在功能医学看来,炎性衰老的来源通常包括:

1.免疫衰老
免疫系统无法有效清除体内的“垃圾”(如错误折叠的蛋白、细胞碎片)。
2.衰老细胞
这些停止分裂但没死的“僵尸细胞”会持续分泌促炎因子(IL-6, IL-1β, MMPs),这被称为SASP(衰老相关分泌表型)。
3.肠道通透性增加
肠道屏障变弱,脂多糖(LPS)入血,触发全身免疫反应。
4.内脏脂肪
腹部脂肪本身就是一个巨大的内分泌腺,不断向外释放炎性因子。
其次,炎性衰老如何摧毁线粒体?
线粒体不仅是“细胞的发电厂”,它也是细胞的“环境感应器”。当身体处于炎性衰老状态时,线粒体会遭受多重打击:
1. 资源掠夺
NAD+的消耗战,这是目前抗衰老研究最热门的机制之一。
• 机制: 炎症(尤其是由CD38酶介导的)会大量消耗体内的NAD+(烟酰胺腺嘌呤二核苷酸)。
• 后果: NAD+是线粒体产生ATP(能量)所必需的辅酶,也是长寿蛋白(Sirtuins)的燃料。
• 结局: 炎症把NAD+“吃光”了,线粒体因为缺乏燃料而熄火。这就解释了为什么慢性炎症患者(如自身免疫病、肥胖)常感到极度疲劳。
2.氧化应激风暴
• 机制:炎症因子激活免疫细胞产生大量的活性氧(ROS)作为武器。
• 线粒体的脆弱性: 线粒体DNA(mtDNA)是裸露的,缺乏像细胞核DNA那样的组蛋白保护,且修复机制较弱。
• 后果: 外源性的ROS直接攻击mtDNA,导致基因突变,破坏电子传递链(ETC),使线粒体产生能量的效率下降,不仅产不出电,反而漏出更多的自由基。
3. 信号通路的拮抗
NF-κB vs. PGC-1α
• NF-κB(炎症总司令): 慢性炎症长期激活NF-κB通路。
• PGC-1α(线粒体生成总司令): 负责制造新线粒体和抗氧化的关键因子。
• 互斥关系: NF-κB能够直接抑制PGC-1α的活性。
• 结局: 只要身体在发炎,线粒体不仅坏得快,而且由于PGC-1α被抑制,身体根本无法制造新的线粒体来补充。这就导致线粒体数量和质量的双重下降。
最后,恶性循环产生,受损线粒体反过来加剧炎症。
这是最可怕的一步。当线粒体受损破裂时,它会释放出内容物(如mtDNA)。
• 演化记忆: 线粒体在几十亿年前是细菌。免疫系统至今仍把线粒体DNA视为“细菌DNA(外敌)”。
• cGAS-STING通路: 泄漏到细胞质中的mtDNA会被cGAS-STING通路识别为“入侵者”,从而触发更猛烈的炎症反应(释放干扰素和细胞因子)。
• 循环建立: 炎症→线粒体损伤→线粒体泄漏→更强的炎症。这就是“炎性衰老-线粒体功能障碍循环”。
三 研究亮点:衰弱状态的动态变化会影响心血管疾病的发展方向
研究显示,从非衰弱状态过渡到衰弱状态的参与者与非衰弱状态的参与者相比,具有更高的发病风险(95%CI:1.34[1.24,1.44]),而从衰弱状态改善到非衰弱状态的参与者,发病风险则显著降低(95%CI:0.70[0.63,0.77])。除此之外,不健康生活方式及行为(吸烟、饮酒、社交隔绝、低频锻炼)也与疾病发生发展关系密切。
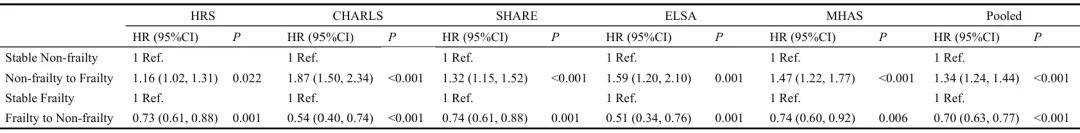
另一个值得注意的发现是,抑郁情绪已成为由衰弱→心血管疾病这一因果链中具有推动作用的因素之一,证实长期的精神压力也会对身体健康造成不利影响。
三 功能医学干预与修复
延缓甚至逆转衰老进程是当前的研究热点之一。对于身处衰弱状态的中老年人,肌肉不仅是运动器官,更是人体最大的抗衰老内分泌器官。通过科学的力量训练配合精准营养,我们实际上是在开具一剂强效的“抗炎与神经修复药”。

首先,从运动角度来看,传统的有氧运动(如散步)虽然好,但不足以逆转肌少症,需要引入多方面且循序渐进的训练模式:
功能医学运动处方(举例):
1. 起步:功能性动作优先
不要一开始就使用复杂的器械。从生活化动作开始,例如:坐站练习(锻炼大腿和臀部,直接关联代谢率)和农夫行走(手提适重物品行走,锻炼核心稳定性和握力)。

2.频率与强度
• 频率: 每周2-3次,给肌肉足够的修复时间(修复即合成)。
• 强度: 必须达到“适度疲劳”,选择的重量应根据自身实际考虑,产生轻度的肌肉酸痛感,才能刺激睾酮(男性)、甲状腺激素、血清素、多巴胺、生长激素等激素的分泌,从而改善抑郁和衰弱。
3.注重离心收缩
• 指导老人在放下重物时要慢(例如3-4秒缓慢动作)。离心收缩对肌肉微结构的刺激最大,且对老年人的心肺负担相对较小。
其次,从营养干预的角度来看,衰弱的老年人普遍存在合成代谢抵抗,这意味着他们吃同样多的蛋白质,合成肌肉的能力却比年轻人差。因此,营养干预需要更“激进”且精准:
1. 蛋白质:数量与时机是关键
• 总量提升: 建议每日蛋白质摄入量达到1.0-1.2克/公斤体重。
• 脉冲式摄入: 仅仅总量够还不行,每餐必须达到启动肌肉合成的“阈值”。建议每餐摄入25-30克优质蛋白(约等于掌心大小的肉/鱼/蛋)。

• 亮氨酸开关: 亮氨酸是启动肌肉合成的“点火钥匙”。对于食欲不佳的老人,可以额外补充支链氨基酸(BCAA)或乳清蛋白粉,因为它们富含亮氨酸,能更容易地穿过血脑屏障,改善中枢疲劳。
2. 必需脂肪酸:给大脑和血管“灭火”
Omega-3脂肪酸(深海鱼油):

• 抗抑郁: 高剂量的EPA(每日1-2克)已被证实具有抗抑郁效果。
• 抗肌少症: Omega-3能增加肌肉细胞对蛋白质的敏感性,帮助老人更好地摄取和吸收。
• 护心: 降低甘油三酯,稳定血管斑块。
3. 关键微量元素:线粒体的燃料
• 维生素D3 + K2: 维D不仅是骨骼维生素,更是神经激素。低维D水平与抑郁症和肌肉无力直接相关。目标是将血清25(OH)D水平维持在50~125nmol/L。

• 镁: 镁是能量代谢的辅酶,也是天然的镇静剂。补充甘氨酸镁或柠檬酸镁可以改善睡眠,缓解焦虑,并支持肌肉功能。
4. 消化支持:确保吃进去能吸收
• 很多老年人因为胃酸分泌减少,吃了肉却消化不了,导致腹胀,反而更不愿意吃蛋白。应该在医生指导下,餐前适当补充甜菜碱盐酸盐或消化酶,这是打破“营养不良-衰弱”循环的第一步。

最后,可以通过积极参加社区活动、培养兴趣爱好等方式增强社会交往能力,或者增加与家人的相处时间,从而减轻孤独或焦虑情绪,使身心处于更加和谐平稳的状态。
总结
年龄的增长不可避免,但身心的强健并不应随年龄而流逝。以肌肉为靶点,营养为燃料,从而调节全身系统,通过这样的功能医学方案,我们不仅能帮助中老年人群降低心血管风险,更能帮助他们重获对生活的掌控感。
参考文献
Zhang Z, Xu H, Zhang R, et al. Frailty and depressive symptoms in relation to cardiovascular disease risk in middle-aged and older adults. Nat Commun. 2025;16(1):6008. Published 2025 Jul 1. doi:10.1038/s41467-025-61089-2
免责声明
该文章只限于科普,仅供学习与交流
不用于任何医疗建议
部分图片来自网络 侵删
