李祥春教授:多模态深度学习模型解锁癌症密码
由中国抗癌协会、天津医科大学肿瘤医院联合主办,Cancer Biology & Medicine、《中国肿瘤临床》两本期刊承办的“第一届 CancerBiology & Medicine 青年学者论坛”于 2025年8月 22日在天津召开。天津医科大学肿瘤医院的李祥春教授作报告了《Unlocking Cancer’s Secrets: Deep Learning from Pixels to DNA for Early Detection and Localization》。《肿瘤瞭望》现将报告主要内容整理如下。
专家简介

李祥春 教授
主要从事生物信息学、肿瘤基因组学和人工智能的研究工作,主持国家自然科学基金项目2项,并入选国家级人才青年项目。在Nature Medicine、Lancet Oncology、JAMA Oncology、Annals of Oncology和Nature Communications等国际权威期刊发表SCI论文30余篇。
人工智能(AI)发展的三大驱动力包括算法(Algorithm)、大数据(Big Data)和计算力(Computing Power)。深度学习模型是当前AI浪潮的核心驱动力,其中CNN(卷积神经网络)和Transformer都是过去十年乃至现在最重要的神经网络框架之一。CNN是计算机视觉的核心。ResNet和DenseNet是深度网络架构设计上的里程碑,ResNet解决深度网络训练中的梯度消失问题,DenseNet将特征复用推向极致。Transformer是所有大语言模型的基础架构,基于自注意力机制。
一、AI在肿瘤起源与诊断中的应用
1
甲状腺癌超声图像诊断
2
桥本甲状腺炎诊断
3
结直肠癌内镜图像诊断
4
全切片图像分类
基于Transformer的全切片图像检测模型(WIT)在TCGA数据集的32种癌症类型检测中达到82.1%的准确率(95%置信区间:80.7%–83.3%),较基线方法显著提升31.6%。研究成果2023年发表于 iScience。
5
肿瘤起源鉴定
基于细胞学的深度学习方法TORCH在肿瘤起源精准定位方面表现出卓越性能。在内部和外部测试集中,TORCH的受试者工作曲线下面积值在癌症诊断0.953 ~ 0.991之间,在肿瘤起源定位0.953 ~ 0.979之间。在整个测试子集、胸腔积液子集和腹腔积液子集中,TORCH模型与资深病理学家的诊断灵敏度均高于初级病理学家。与TORCH预测一致的治疗方案带来更好临床获益。研究成果2024年在Nature Medicine发表。
6
食管鳞癌新的驱动基因与酒精摄入突变特征
该研究发现中国人食管鳞癌新的驱动基因与酒精摄入突变特征:食管鳞癌中新的驱动基因和T>C突变特征跟酒精摄入密切相关,为食管鳞癌的发生发展和防控提供了新的见解。该研究于2018年发表在Annals of Oncology。
二、AI在cfDNA液体活检中的应用
cfDNA是细胞凋亡/坏死释放的循环DNA片段,在癌症早筛、治疗监测、移植排斥监测、无创产前检测等有应用价值。传统cfDNA分析方法依赖序列比对、甲基化等特征,存在CNV、VAF假阳性、忽略有用信息等问题。报告介绍了几种新方法:
☆基于序列比对的生物信息学方法:
DELFI —— 整合片段组学特征
CancerSEEK —— 体细胞突变+血浆蛋白标志物
☆非比对统计分析方法:
MDS —— cfDNA末端模体多样性分析
NMF —— cfDNA末端模体特征谱解析
☆端到端人工智能解决方案:
李祥春团队方法:DECIDIA、EMIT、ACID和iLLMAC。
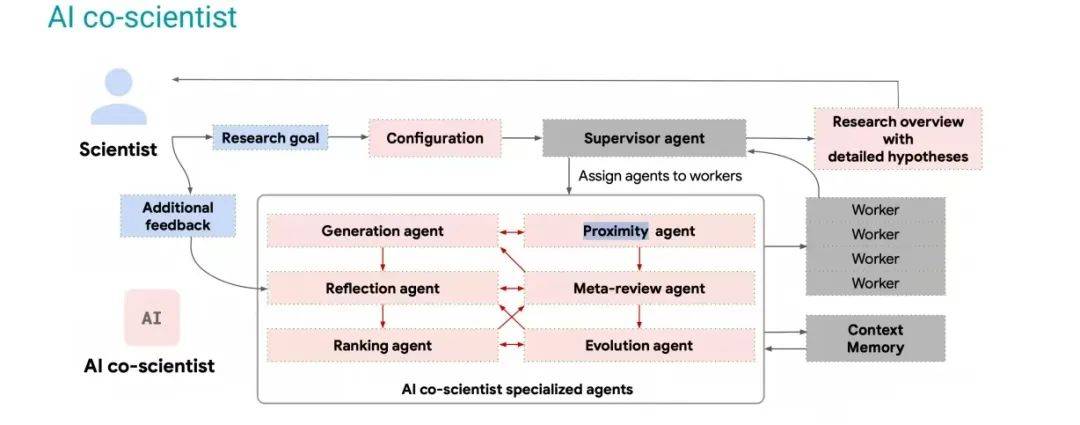
三、AI作为科研合作者