告别 “减重难”:GLP-1 类药物之后,肥胖治疗还有这些新方向
▲体内CAR疗法-全球研究与发展格局(2025)免费领取!
摘要: 肥胖作为一种慢性疾病,全球患病人数约 6.5 亿,还会引发 2 型糖尿病、心血管疾病等多种并发症。过去,生活方式干预减重效果有限且易反弹,减重手术虽效果好却难以普及。如今,随着对肠 - 胰激素调节体重机制的深入研究,肥胖治疗进入新阶段。以 GLP-1 受体激动剂为基础的多款新药涌现,部分药物减重效果接近减重手术,还能改善代谢指标。本文将详细介绍这些新型肥胖治疗药物的研发进展、效果与挑战。

一、肥胖治疗的现状与困境
肥胖是全球高发的慢性疾病,全球约有 6.5 亿人受其困扰,它会显著增加患 2 型糖尿病(T2D)、代谢相关脂肪性肝病(MASLD)、心血管疾病、骨关节炎等并发症的风险。
在过去,生活方式干预(包括饮食控制、运动和行为调整)是肥胖管理的基础,但其减重效果有限,即使是高强度干预,平均减重也仅能达到 10%,且 5 年内 80% 的减重成果可能反弹。这主要是因为大幅减重后,人体基础代谢率降低,食欲反而增加,背后还涉及食欲促进信号增强、食欲抑制信号减弱等生理机制。
而减重手术虽能实现 25%-30% 的平均减重,且效果持久,却因手术风险、费用较高以及人们对手术的顾虑,无法在人群中大规模推广。
此前获批的GLP-1 受体激动剂(如每周注射一次的司美格鲁肽 2.4mg),能通过抑制食欲实现 15%-17% 的平均减重,还具有心血管保护作用,但与减重手术效果仍有差距,且目前多为注射剂型,部分患者接受度不高。
二、新型肥胖治疗药物管线:从单药到联合
随着对肠 - 胰激素(如 GLP-1、GIP、胰高血糖素、胰淀素等)调节食欲和血糖机制的深入研究,多款新型肥胖治疗药物进入临床阶段,主要分为以下几类:
(一)口服 GLP-1 受体激动剂
为解决注射剂型的不便,科研人员研发出口服 GLP-1 受体激动剂。其中,口服司美格鲁肽 50mg已完成 III 期临床试验(OASIS-1),在无 2 型糖尿病的肥胖人群中,结合中等强度生活方式干预,68 周内平均减重 17.4%,而安慰剂组仅减重 1.8%,同时还能改善血压、血脂等心血管风险指标(表 2)。另一款口服药物奥福格列肽,无需空腹服用,便利性更高,II 期临床试验显示,36 周内最高可实现 14.7% 的减重(表 2)。
(二)肠 - 胰激素联合激动剂
双受体激动剂
替尔泊肽(GLP-1/GIP 双受体激动剂):已获美国 FDA 和欧洲 EMA 批准用于肥胖治疗,III 期临床试验(SURMOUNT-1)显示,无 2 型糖尿病的肥胖人群 72 周内平均减重 16%-22.5%,部分患者甚至能维持减重效果不反弹(图 3)。对于合并 2 型糖尿病的肥胖患者,也能实现 15.7% 的平均减重,同时显著降低糖化血红蛋白(HbA1c)(表 3)。
卡格列肽/司美格鲁肽复方制剂(GLP-1/胰淀素双受体激动剂):II 期临床试验显示,肥胖人群 20 周内平均减重 17.1%,效果优于单独使用司美格鲁肽(表 2)。
苏沃杜肽、马祖杜肽(GLP-1 / 胰高血糖素双受体激动剂):苏沃杜肽 II 期临床试验中,肥胖人群 46 周内最高减重 18.7%;马祖杜肽在我国肥胖人群中的 II 期试验显示,24 周内最高减重 11.3%,更高剂量(9mg)的试验还在进行中(表 1、表 2)。
三受体激动剂瑞他鲁肽(GLP-1/GIP/ 胰高血糖素三受体激动剂)是目前减重效果最显著的在研药物之一,II 期临床试验中,无 2 型糖尿病的肥胖人群 48 周内平均减重最高达 24.2%,接近减重手术效果,同时还能改善血脂和血压(表 2、图 3)。
(三)非肠 - 胰激素类药物
比马鲁单抗是一类新型药物,通过阻断激活素 II 型受体促进骨骼肌生长,在 II 期临床试验中,合并 2 型糖尿病的肥胖人群 48 周内脂肪量减少 20.5%,同时增加 3.6% 的肌肉量,避免了减重过程中肌肉流失的问题(表 3)。
表1 未来肥胖治疗药物管线
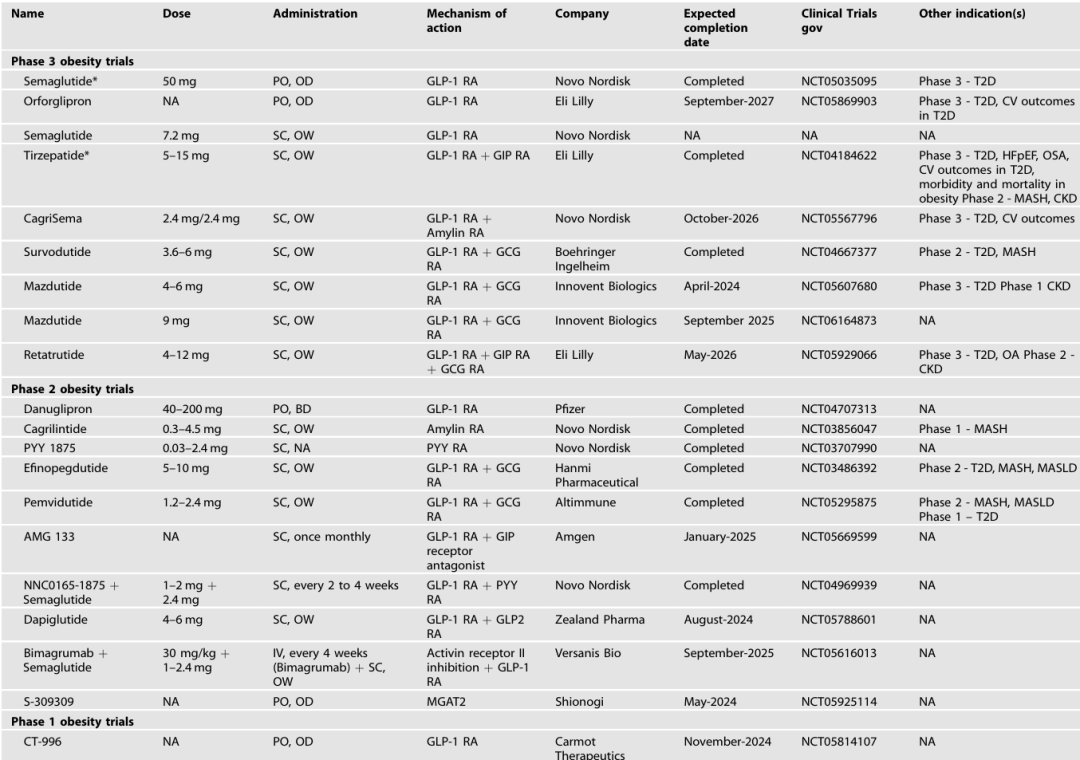
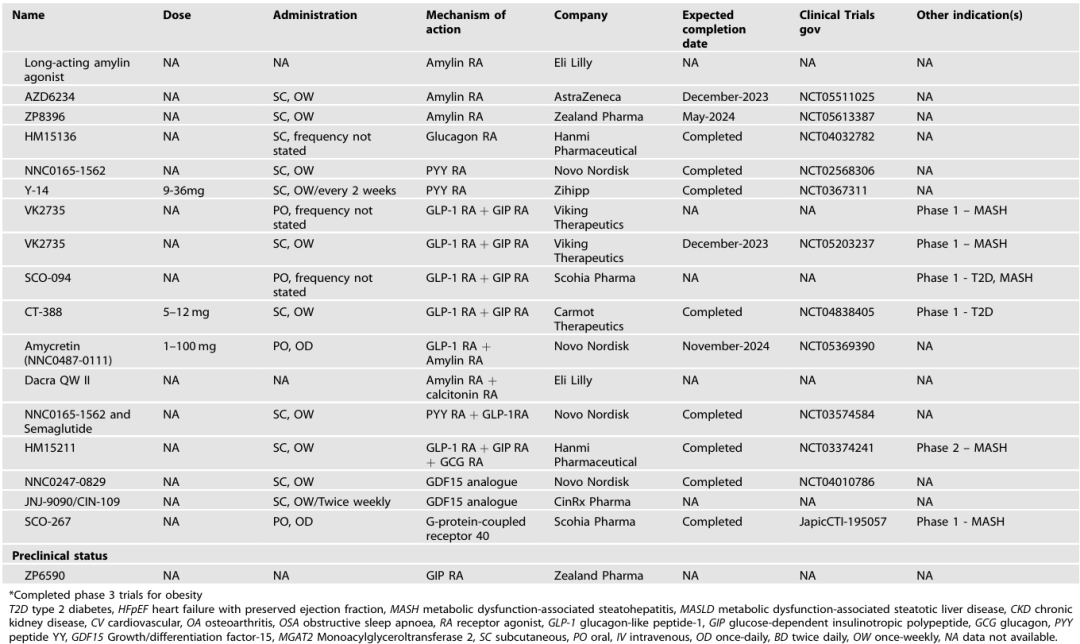
表 2 无 2 型糖尿病人群中肥胖治疗药物的疗效与安全性
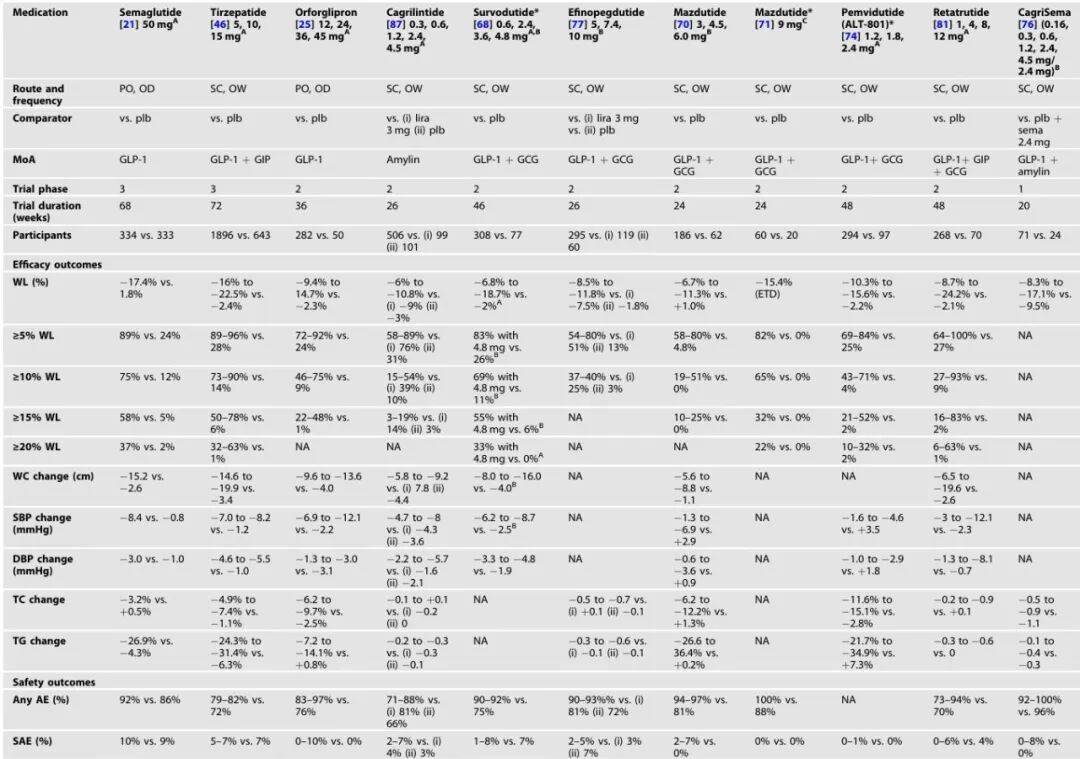
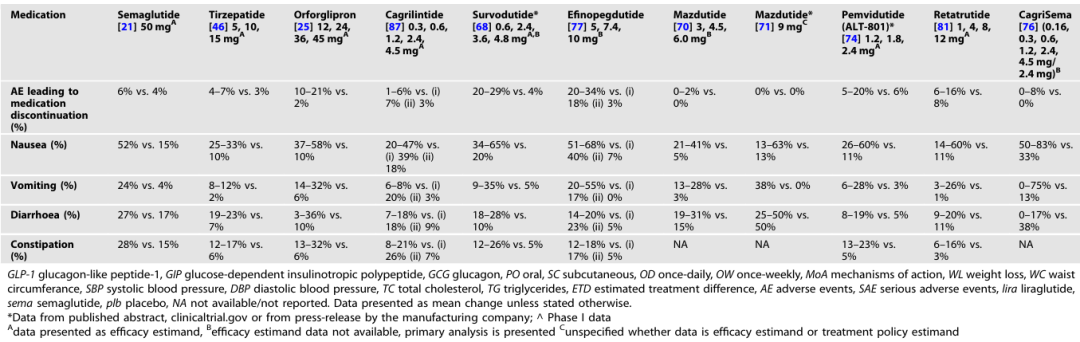
表3. 2型糖尿病患者管道分子治疗的有效性和安全性结果
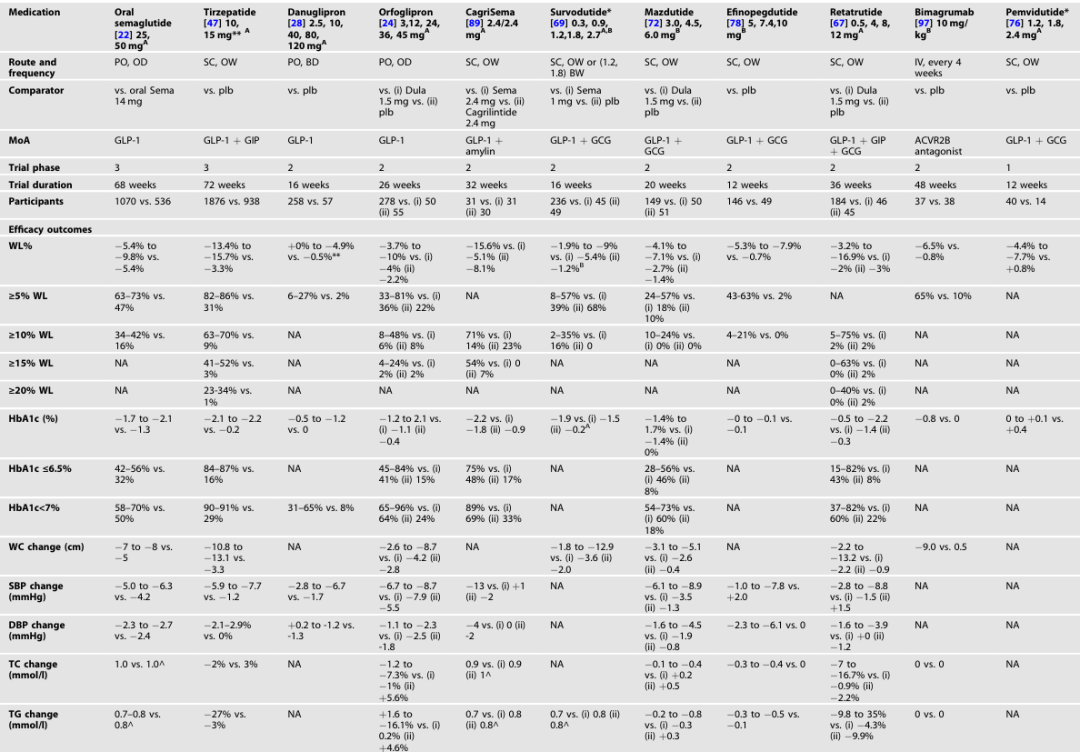
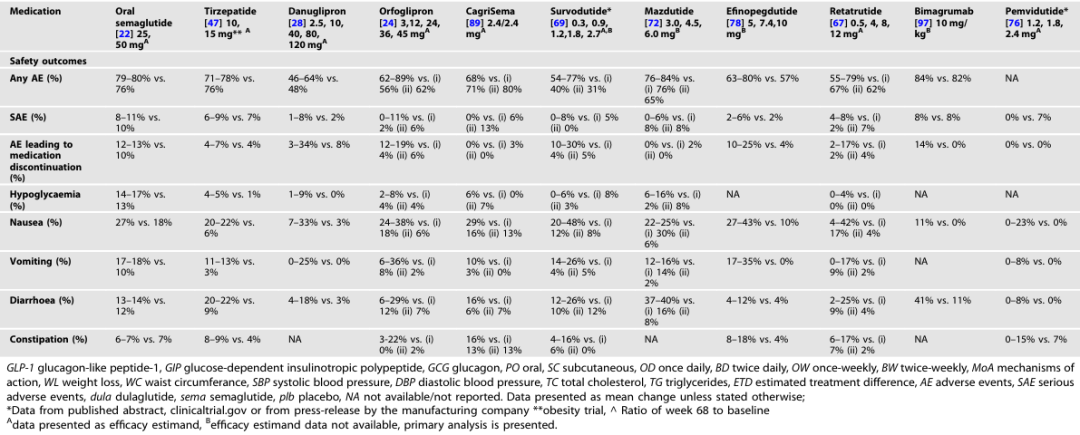
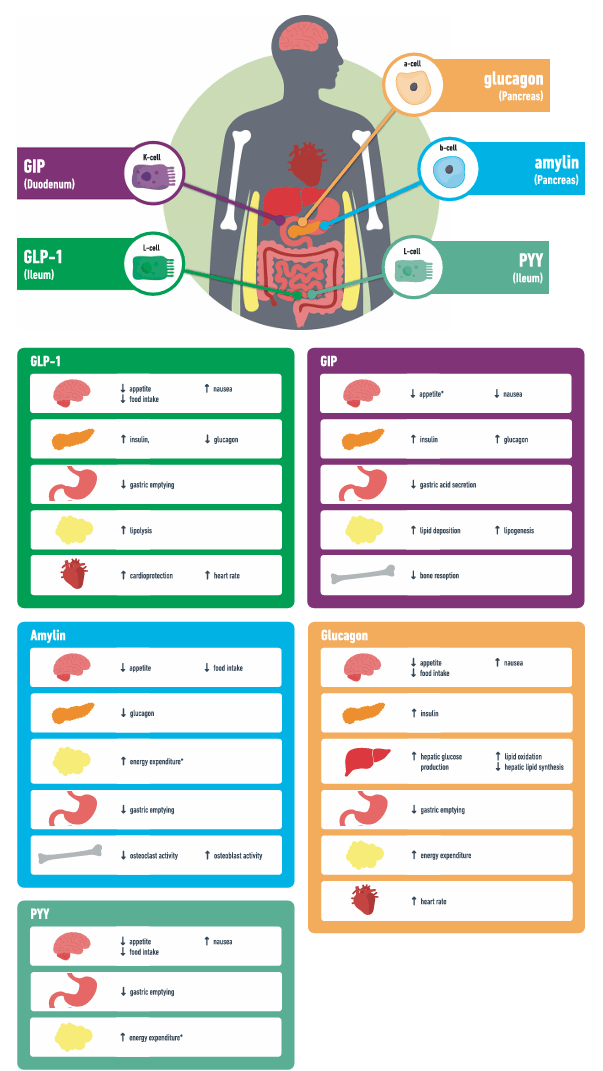
图 1 用于肥胖治疗管线的肠道激素分泌及主要作用
图 1 内容:展示了胰高血糖素(胰腺分泌)、GIP(十二指肠分泌)、胰淀素(胰腺分泌)、GLP-1(回肠分泌)、PYY(回肠分泌)等肠道激素的分泌部位及主要作用,如调节血糖、食欲等
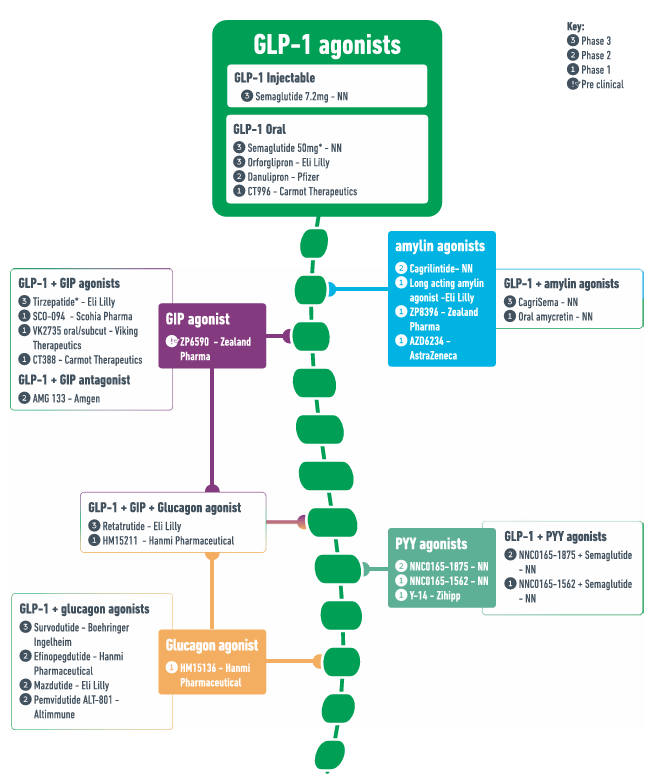
图2 以 GLP-1 为基础的肠道激素类肥胖治疗药物管线
图 2 内容:呈现了 GLP-1 激动剂(注射型、口服型)、GLP-1+GIP 激动剂、GLP-1 + 胰淀素激动剂、GLP-1 + 胰高血糖素激动剂、三受体激动剂等各类药物的研发阶段和相关企业
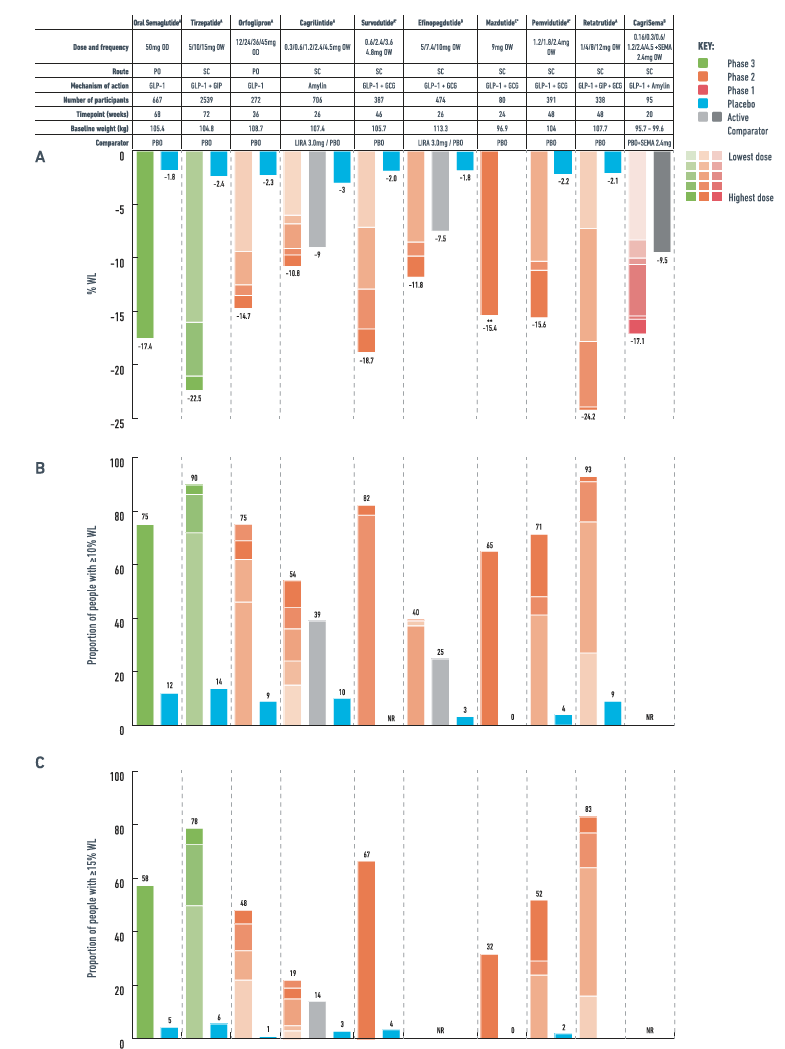
图3 无糖尿病人群中肥胖治疗药物的减重效果
图 3 内容:A 图为平均减重百分比,B 图为实现≥10% 减重的人群比例,C 图为实现≥15% 减重的人群比例,展示了不同药物的减重效果差异
三、新型药物的临床意义与挑战(一)临床意义
减重效果逼近手术:多款新型药物(如瑞他鲁肽、替尔泊肽)的减重效果已达到 20% 以上,接近减重手术,为无法或不愿接受手术的患者提供了新选择。
改善并发症:这些药物不仅能减重,还能降低糖化血红蛋白、改善血脂、血压,对 2 型糖尿病、MASLD 等并发症有治疗作用。例如,替尔泊肽能减少 40%-47% 的肝脏脂肪含量。
个体化治疗成为可能:不同机制的药物(如 GLP-1 类、肌肉保护类)可根据患者的合并症、偏好(口服或注射)等因素选择,实现个体化治疗。
(二)面临挑战
不良反应:多数药物的常见不良反应为胃肠道反应(如恶心、呕吐、腹泻),部分药物(如 GLP-1/胰高血糖素双受体激动剂)因不良反应导致的停药率较高(20%-30%)。
长期安全性未知:目前多数临床试验随访时间较短(1-2 年),药物长期使用的心血管安全性、对骨骼健康的影响等仍需进一步研究。
可及性与成本:新型药物价格较高,未来如何通过医保覆盖、技术迭代降低成本,确保更多患者获得治疗,是重要挑战。
四、总结
肥胖治疗已进入 “多药物、多机制” 的新时代,以肠 - 胰激素联合激动剂为代表的新型药物,在减重效果和并发症改善上取得重大突破,部分药物效果已逼近减重手术。未来,随着更多 III 期临床试验完成、长期安全性数据公布以及药物可及性提升,肥胖管理将实现从 “基础干预” 到 “精准治疗” 的转变,为全球 6.5 亿肥胖人群带来新希望。但同时,也需关注药物不良反应、长期安全性和成本问题,推动肥胖治疗向更安全、有效、可及的方向发展。
