孕前期抗生素暴露影响子代肠道健康!北医三院消化科段丽萍教授团队在Advanced Science发表成果
2026年4月2日,北京大学第三医院消化科段丽萍教授团队在Advanced Science(IF:14.1)上发表了题为“Maternal Preconception Antibiotic Exposure Disrupts Microbial Succession: A Transgenerational Risk for Offspring Gut Mucosal Immaturity and Colitis Susceptibility”(母体孕前期抗生素暴露扰乱微生物演替是子代肠道黏膜发育不良及结肠炎易感性的跨代风险因素)的研究成果。

生命早期微生物组在宿主发育和终生健康中起着关键作用。越来越多的研究发现,母体因素在塑造子代微生物组方面至关重要。然而,孕前期母体健康对子代的影响仍未被充分研究。
针对孕前期微生态扰动对后代健康影响不明的问题,本研究结合动物实验与临床队列,利用多组学及粪菌移植技术,探究了母体孕前期抗生素暴露对后代肠道微生态及结肠炎易感性的跨代影响,揭示了母体孕前期健康是子代健康的跨代际风险因素,因此,在常被忽视的孕前期也应谨慎使用抗生素。
1
动物实验
研究证实了孕前期抗生素暴露的长期后果。母鼠仅在孕前接受一周的广谱抗生素处理,其子代从幼年期到成年期,肠道黏膜结构始终呈现“不成熟”状态,具体表现为回肠绒毛缩短、结肠隐窝变浅、杯状细胞减少,以及紧密连接蛋白表达下调。
这种由孕前期抗生素暴露导致的子代肠道屏障脆弱性,使其在成年后面对低剂量化学刺激时,表现出更严重的结肠炎症状。
2
宏基因组和代谢组学分析
研究团队发现,孕前期抗生素暴露不仅重塑了母鼠自身的肠道微生态,更将这种“紊乱印记”通过肠道菌群的跨代际传递,牢固地烙印在子代的肠道生态中。
孕前抗生素暴露通过增强母–子代间的微生物传递、改变微生物的发育轨迹,以及增加微生物群落组装过程中的选择压力,诱导了子代微生态的长期紊乱。
通过粪菌移植实验证实,将这种“紊乱”的子代菌群移植给无菌小鼠,使其在面对低浓度刺激时,表现出与供体相似的、显著增强的疾病易感性。
这强有力地证明了,孕前期抗生素暴露通过重塑子代菌群,导致子代结肠炎风险升高这一核心机制。这些改变最终导致了子代持续性的肠道黏膜发育不良,并显著提高了成年后结肠炎的易感性。
3
补充性的临床研究
结果显示,炎症性肠病(IBD)患儿及其临床表型健康的母亲,两者的肠道微生物组与代谢组呈现出一致的改变,特征为促炎性菌群和代谢物的富集。
值得注意的是,IBD患儿的母亲所报告的抗生素暴露水平显著高于对照组,这种暴露同样与母–子代间微生物传递增强、微生物群落组装过程中的选择压力增加相关。这些数据提示,在人类中可能也存在类似的、由母体抗生素暴露驱动的菌群跨代紊乱机制。
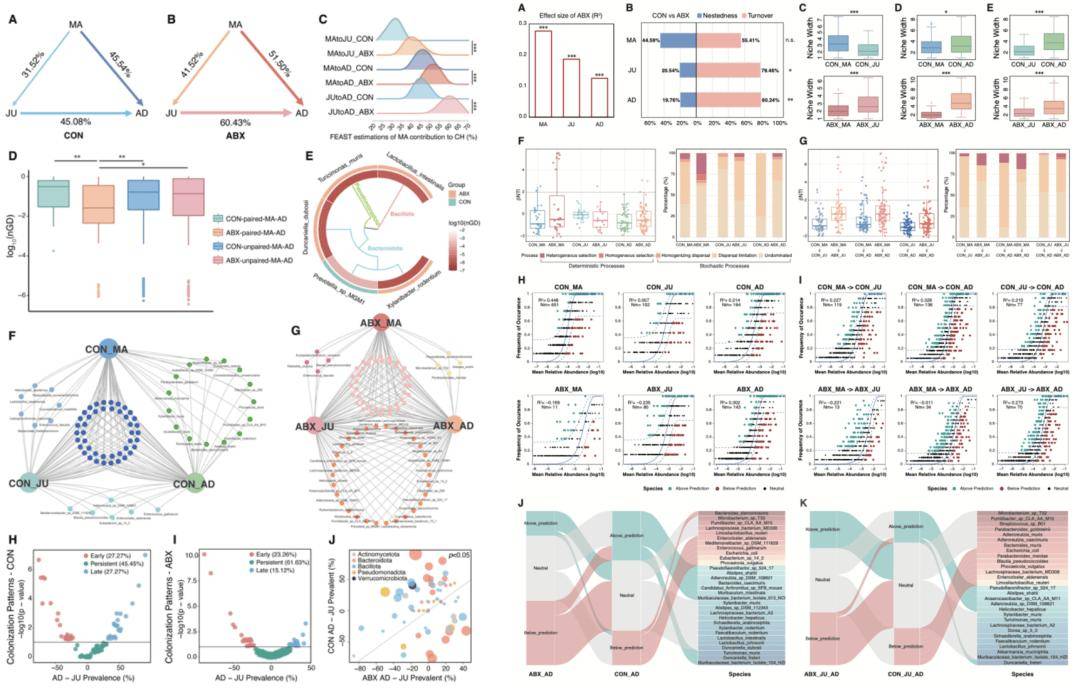
母体孕前期抗生素暴露跨代际影响子代健康的潜在机制
本研究首次系统揭示了孕前期这一关键窗口期,母体微生物组对后代肠道发育和长期健康的奠基性影响。它强调,抗生素的谨慎使用不应仅限于孕期,而应前移至备孕阶段。这项发现为从生命最早起源阶段预防炎症性肠病等免疫相关疾病,提供了全新的科学视角和潜在的干预靶点。
北京大学第三医院消化科博士研究生陈俞竹、助理研究员段汝乔、博士研究生张存正为该论文共同第一作者,消化科段丽萍教授为该论文的通讯作者。本研究得到国家重点研发计划、国家自然科学基金及北京市自然科学基金的支持。
共同第一作者
陈俞竹
消化科2022级博士研究生
主要研究方向:
肠道微生态与胃肠道疾病(医学创新交叉)

段汝乔
消化科助理研究员、住院医师
主要研究方向:
肠道微生态、神经胃肠病学

张存正
消化科2024届博士研究生
主要研究方向:
肠道微生态与肠神经系统发育

通讯作者

段丽萍
北京大学第三医院
大内科主任
消化科主任医师、教授、博士生导师
主要研究方向:消化系统疾病的诊断与治疗,重点研究领域为神经胃肠病及肠道微生态。
文 | 消化科 陈俞竹
审核 | 科研处
编辑 | 宣传中心 张轩烨
