AI辅助药物研发:糖尿病视网膜病变口服疗法在路上
原创 青白视角 Aggie 青白视角
2024年7月12日 14:15 浙江

笔者曾在美国眼科创新热点:2015-2020专利趋势分析一文中结语写到:“另外,笔者也特别关注到,远程医疗和基于人工智能的诊断、药物发现等技术在美国专利趋势中并未得到突出反映,但众所周知,中国在数字技术领域的创新和产业化全球领先,同时中国未来人口结构的老龄化问题尤为凸显,因此这个领域或许是我们可以实现弯道超车的细分赛道之一......“本文提及的技术和案例正验证了笔者上述观点。

前言
对接(Docking)是一种用于药物发现的计算技术,用于预测小分子(候选药物)与目标蛋白质相互作用的“程度”。对接在药物发现的早期阶段至关重要,因为它能够高效筛选大量化合物库,节省时间和资源。近年来,基于人工智能的方法已成为分子对接的有前途的替代方案,具有高精度的潜力,而无需承担过高的计算成本。在全球范围内,分子对接市场是更广泛的药物发现信息学市场中的一个重要部分,预计该市场将从2023 年的30 亿美元增长到 2032 年的80 亿美元,这得益于制药公司对研发投资的增加和先进计算工具的采用。
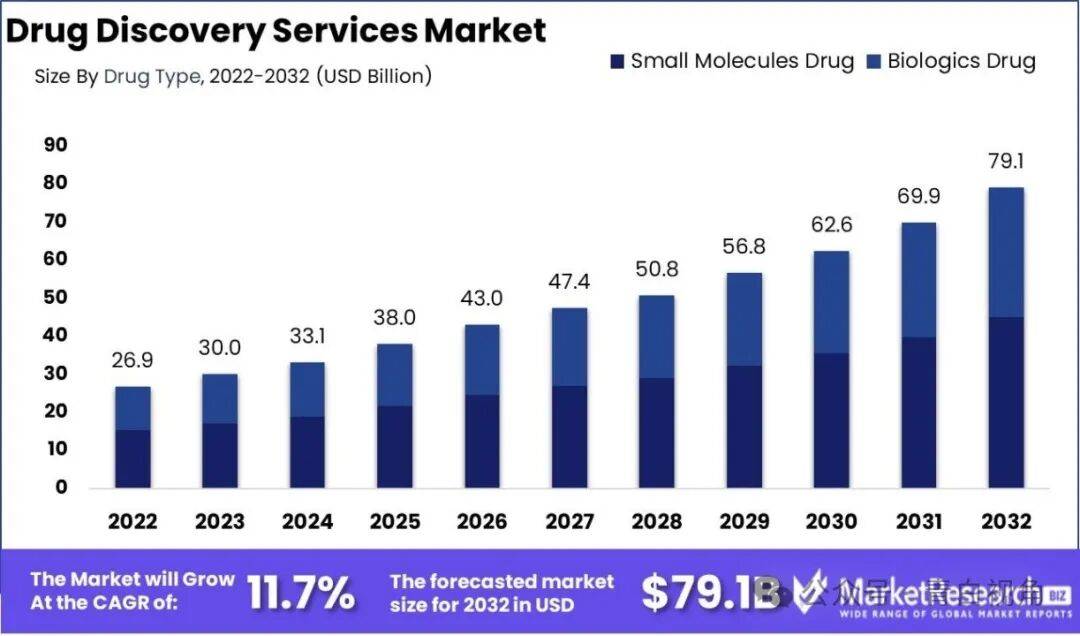
对接技术已从传统的基于物理/评分的方法发展到先进的基于深度学习/人工智能的方法。最初,对接依靠物理和化学原理来预测相互作用,使用评分函数根据几何和能量因素来评估结合亲和力。深度学习的出现使模型能够直接从数据中学习复杂的分子表征,从而改变了对接。这些深度学习模型可以捕捉以前难以建模的复杂模式和相互作用,从而实现更准确、更有效的预测。

AI在眼科药物研发中的应用
基于人工智能的药物对接技术,在眼科疾病的药物研发中取得了显著进展。近日,国内深势科技(DP Technology )宣布 DPT0415 被提名为治疗糖尿病视网膜病变 (DR) 和糖尿病黄斑水肿 (DME) 的临床前候选化合物。
2.1 Lp-PLA2 及其在DR和DME中的作用
DR 是糖尿病引起的微血管并发症,也是中老年人视力丧失的主要原因。1/3的糖尿病患者患有 DR。DME 可发生在 DR 的任何阶段,其原因是血视网膜屏障破裂导致黄斑中过多的液体和脂质积聚。抗VEGF药物的出现彻底改变了 DME 的治疗。然而,许多患者尽管尝试多次注射药物,仍未完全控制疾病,这可能是因为 DR 也是一种炎症性疾病,许多细胞因子和趋化因子参与了这一过程。因此,应探索 VEGF 以外的分子机制。
Lp-PLA2 属于 PLA2 超家族第 VII 组,主要由巨噬细胞分泌,与低密度脂蛋白 (LDL) 和高密度脂蛋白 (HDL) 形成复合物在血液中循环。Lp-PLA2 水解氧化磷脂,通常在低密度脂蛋白 (LDL) 上水解,生成溶血磷脂酰胆碱 (lysoPC)。LysoPC 会诱发血管炎症,导致血视网膜屏障 (BRB) 受损。
2015年葛兰素史克曾探索过作为 Lp-PLA2 抑制剂的达拉帕地(Darapladib)的口服疗法。在一项糖尿病性黄斑水肿 (DME) IIa 期研究中,研究结论显示: 每日口服一次达拉帕地 3 个月可显著改善视力和黄斑水肿,值得进一步研究这种新型脂蛋白相关磷脂酶 A2 抑制机制在治疗 DME 方面的作用。

2.2 DPT0415 的临床前研究
DPT0415 是一种高效、选择性强且安全的 Lp-PLA2 抑制剂,具有新颖的结构。它在 0.3 mpk 时表现出足够的靶标参与度,并在 STZ 诱发的大鼠 DR 模型中控制了视网膜病变的进展。该化合物比达拉帕地具有更高的效力、更好的 ADME (药物吸收Absorption、分布Distribution、代谢Metabolism和外排Excretion的简称)和物理化学性质,并在临床前研究中展现出足够的安全性。
目前,DME 的标准治疗方法是眼部注射 VEGF 抗体以保护视力。由于这种给药方式具有侵入性,患者往往会将治疗推迟到疾病的后期。作为治疗 DME 的口服疗法,DPT0415 可以通过靶向 Lp-PLA2 来治疗炎症和血管渗漏,从而改善视力。此外,Lp-PLA2 抑制剂 DPT0415 有可能通过在早期治疗 DME 来显著改变治疗模式,从而获得更好的疗效。
2.3 深势科技
2.3.1 技术平台、底层模型
深势科技成立于2018年,总部位于北京,是 AI for Science 范式的领先企业,致力于整合“AI + 模拟 + 实验”来解决尚未满足的医疗需求。DPT0415 的成功发现得益于 RiDYMO® 平台中的 Uni-FEP 和 Uni-QSAR 等多个模块,以优化药效和 ADME 特性。该公司依托基于动态机制的药物设计平台RiDYMO®,建立了全球领先的药物发现平台,重点关注中枢神经系统、肿瘤和自身免疫性疾病三个领域。
RiDYMO®难成药靶标研发平台集成多种AI与物理算法,致力于针对“不可靶向”靶点和“最佳”分子进行药物开发。作为其核心算法之一的强化动力学(RiD)在分子动力学模拟的采样效率方面具有显著优势,充分利用神经网络的高维表征能力,高效捕捉复杂生物分子系统中的动态构象变化。
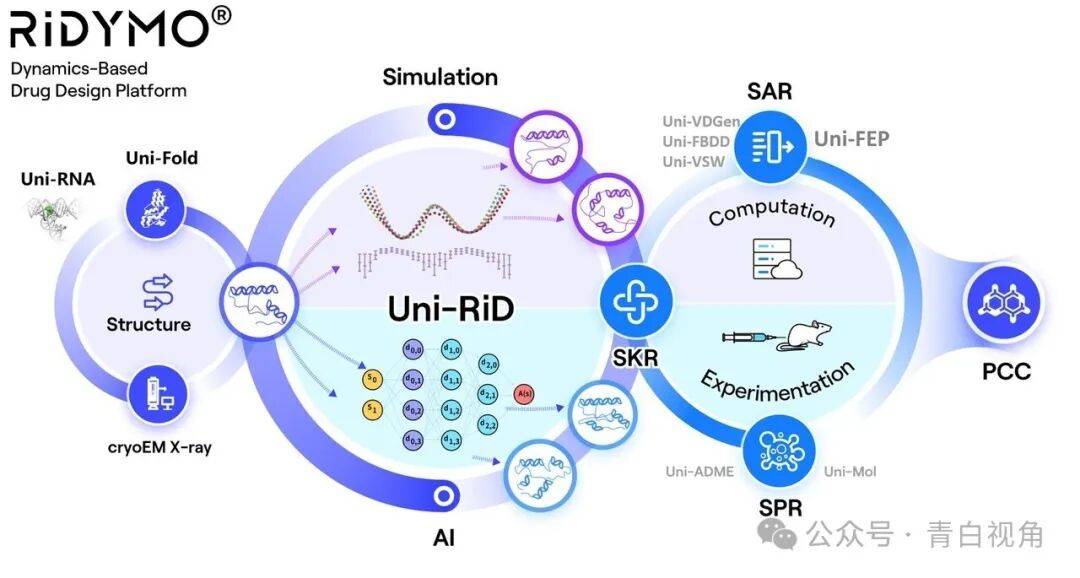
为了推动人工智能在科学领域的应用,深势科技开源了其强大的基于人工智能的 Uni-Mol Docking v2 模型,并将其提供给科学界。Uni-Mol Docking v2 是一个在 AlphaFold3 之前发布的功能强大的对接模型。
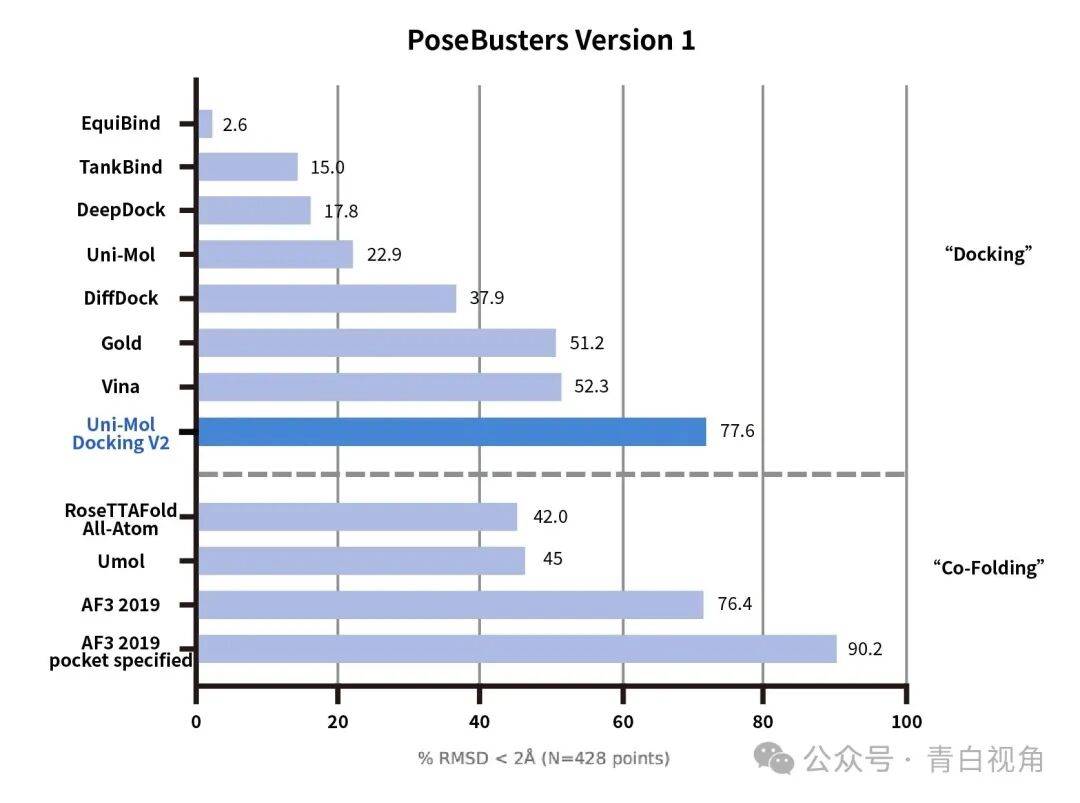
Uni-Mol Docking v2 基于深势科技开发的预训练 AI 模型。Uni-Mol 在各种任务上取得了最先进的结果,表明其具有泛化能力,并使其成为分子任务的强大基础模型。Uni-Mol Docking v2 在 CASF-2016 基准测试中与传统对接算法(如 Autodock Vina)相比取得了卓越的性能。Uni-Mol Docking v2 在预测结合姿势方面具有更高的准确性,超过 77% 的配体的 RMSD 值低于 2.0 Å,超过 75% 的配体通过了所有质量检查。这标志着准确率从 62% 大幅提升,也超越了其他已知的开源方法
深势科技的业务版图不仅仅在医药领域,其依托在交叉学科领域深耕,构建了“深势·宇知®”AI for Science大模型体系,将众多学科的科研方法从“实验试错/计算机”时代带入了“预训练模型时代”,机器“微观尺度工业设计与仿真”为切入点,除打造了Hermite®药物计算设计平台、RiDYMO®难成药靶标研发平台外,也构建了Bohrium®玻尔科研空间站及Piloteye®电池设计自动化平台等科研和工业研发基础设施,形成了AI for Science的“创新-落地”链路和开放生态,赋能“千行百业”,为生物医药、能源、材料和信息科学与工程研究打造新一代工业设计与仿真系统。
2.3.2 融资情况
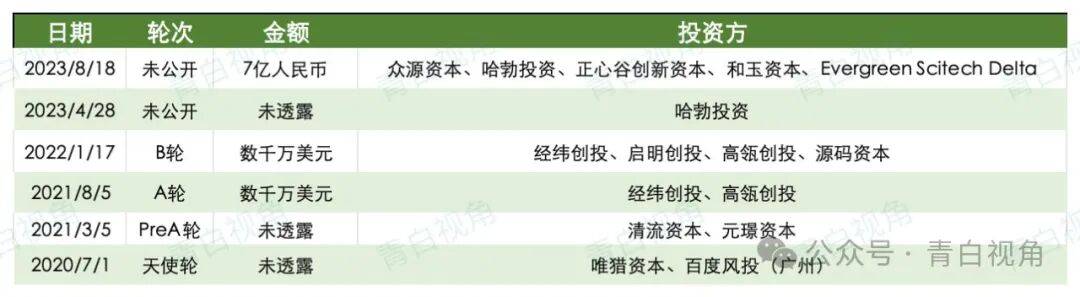
数据源:药融云,制表:青白视角

结语
通过将人工智能与分子对接技术相结合,DPT0415 的成功发现展示了人工智能在药物发现中的巨大潜力,推动了眼科领域的药物研发。未来,期待国内更多深势科技出现,通过开放科学和协作来加速发现,并在全球范围内推动各个领域的有意义的进步。
补充:创新口服视网膜疗法热度有增无减「1」
以下简单罗列几种创新口服视网膜疗法(有数十种)。适应证方向主要在糖尿病视网膜病变、黄斑变性和斯塔加特病等视网膜疾病。
3.1 AKST4290(Alkahest)
AKST4290是一种每日两次口服的趋化因子 CC 基序受体 3 (CCR3) 抑制剂,嗜酸细胞趋化因子是一种免疫调节蛋白,随着人类年龄的增长导致特定的年龄相关疾病。AKST4290可减少新诊断、未接受治疗的湿性AMD的标志性炎症和新生血管形成。
3.2 ALK-001(阿尔克斯制药)
ALK-001 是维生素 A 的口服改良形式,旨在减缓有毒维生素 A 聚集体或“二聚体”的形成,而有毒维生素 A 聚集体或“二聚体”会导致这些疾病。ALK-001 用于治疗继发于干性 AMD 的GA 和Stargardt 病。
3.3 LBS-008(Belite Bio )
LBS-008 为一种针对干性 AMD 的一流口服小分子血清视黄醇结合蛋白 4 (RBP4) 特异性拮抗剂。LBS-008 减少循环系统维生素 A 的水平,从而减少向眼睛递送,适应证为干性 AMD 和 Stargardt 病。
3.4 Xiflam(OcuNexus)
Xiflam 是一种口服小分子药物,一种连接蛋白半通道阻滞剂,可阻断连接蛋白 43 (Cx43) 半通道,该半通道已被证明在渗出性视网膜疾病中过度表达。该化合物于 20 年前开发用于偏头痛治疗后因公司合并而停止了开发。现在适应证为DME、湿性 AMD 和 GA。
3.5 OCX063 (Occurx)
OCX063 一种口服抗炎抗纤维化药物,用于治疗增殖性玻璃体视网膜病变、nAMD 和非增殖性糖尿病视网膜病变 (NPDR)。
3.6 RZ402(Rezolute Bio)
RZ402 是一种每日一次的口服疗法,针对激肽释放酶-激肽系统,抑制血浆激肽释放酶,从而阻断下游缓激肽的产生以及导致 DME 的并发症。
3.7 酪氨酸激酶抑制剂X-82 (Tyrogenex)
一种口服酪氨酸激酶抑制剂,对VEGF 受体 (VEGFR) 和血小板衍生生长因子受体 (PDGFR) 有活性,眼部适应证为 nAMD。
3.8 danegaptide(Breye)
通过靶向细胞间的间隙连接来维持血管结构的完整性,防止由高葡萄糖应激条件引起的细胞间解偶联、视网膜毛细血管破裂和血管渗漏。这药物已经在用于治疗心肌梗塞的临床试验中表现出良好的安全性。眼部适应证为DR、DME、AMD 。
参考
1、青白视角|又一口服视网膜疗法启动临床:一直在路上
